- JMP User Community
- :
- Blogs
- :
- JMP Blog
- :
- 臨床試驗中不良事件資料的視覺化評價
- Subscribe to RSS Feed
- Mark as New
- Mark as Read
- Bookmark
- Subscribe
- Printer Friendly Page
- Report Inappropriate Content
新藥上市前後的各種臨床研究的目的之一是藥物安全性評價,安全性評價的指標包含生命體征指標測量、實驗室檢查、和不良事件觀察等。目前對於不良事件的分析停留在描述不良事件發生率和列舉不良事件清單上,尚不能滿足臨床研究安全性評價的需要。本文試圖從統計描述的角度,在不良事件分析中引入視覺化方法,該方法是把不良事件觀察到的資料轉換為靜態或動態圖像圖形,發現隱含在資料中的藥物安全性信號,為理解資料、分析資料、形成概念、找出規律提供幫助。本文共展示6種圖形:森林圖、樹圖、火山圖、韋恩圖、存活函數圖和風險函數圖,我們將結合不良事件分析目的對圖形設計和解釋展開討論。
1. 研究背景
1.1 不良事件的定義
不良事件(adverse event,AE)的定義為:患者或臨床試驗受試者接受一種藥品治療後出現的不良醫學事件,但並不一定與藥物有因果關係。其中對臨床試驗過程中發生的需要住院治療、延長住院時間、傷殘、影響工作能力、危及生命或死亡、導致先天畸形等特定的不良事件定義為嚴重不良事件(serious adverse event,SAE)。對按規定劑量正常應用藥品的過程中,產生的有害的而非期望的、與藥品應用有因果關係的不良事件稱為藥物不良反應(adverse reaction,ADR)。
1.2 不良事件資料的記錄
臨床試驗中不良事件的記錄是有既定的標準,目前也有推薦使用臨床資料交換標準協會(Clinical Data Interchange Standards Consortium ,CDISC)所提出的標準。CDISC中的臨床資料獲取標準(Clinical Data Acquisition Standards Harmonization ,CDASH)指出不良事件的收集必須包含以下內容:不良事件名稱、開始時間、結束時間、是否嚴重不良事件、與藥物的關係、採取的措施、結局和嚴重程度。可以根據需要選擇性收集不良事件分類、不良事件模式、不良事件編碼以及不良事件系統分類等資訊。
1.3 不良事件分析
當前不良事件分析最簡單的方法是根據發生不良事件的病人數除以接受研究治療的病人總數而得到的粗率。粗率能反映不良事件的發生的基本情況,但是難以反映所發生不良事件的細節和特點,粗率計算還有一個缺點是未考慮暴露時間,為了顧及暴露時間,我們可以考察每單位暴露時間下的事件發生情況,其定義為發生特定事件的例數與病人暴露到發生時間或試驗結束的各病人暴露總時間的比值。籠統地或者單個地分析不良事件的常規做法不容易獲得安全性的全貌,有學者提出對安全性資料按機體系統分類。ICH-E3中給出的不良事件的列舉形式不僅要求描述總的不良事件經歷,還要列舉出所有的不良事件。統計表中應列舉每種不良事件,各組對應的例數和率;還應按機體系統對不良事件分類;區分不良事件是否與研究治療有關;必要時還應按不良事件的嚴重程度進行分類。發生率較高的不良事件和組間差異較大的不良事件應該詳細描述。
1.4 不良事件的視覺化評價
通過一些視覺化方法進行系統、全面的不良事件分析,圖形可以簡潔的傳達多方面的資訊,尤其是基於最近年發展的一些新技術,比如森林圖、樹圖、火山圖、韋氏圖等,圖形比表格更能有效傳達資訊。再者,圖形可以把資料的統計描述與其相應的統計量整合到一起。在探索性臨床試驗中圖形可以説明發現異常安全信號,在確證性臨床試驗中,圖形可以説明我們解釋和闡述已知安全性問題。
不良事件的視覺化表達具有很多優點。第一,減少漏失信號的可能性,提高了儘早發現的可能性。第二,從人的生理角度來講,圖形通過激發人眼的各種潛能---快速、高頻的識別與處理,對相關內容的認知與關聯,暫態不費力的達到處理資訊的目的,一個圖形在呈現時無需太多的解釋和推理過程,就能直接進入人的心理空間。第三,設計良好的圖形可以統計師與臨床研究項目團隊中的其它同事,醫生的溝通能力。第四,統計圖形不僅可以更快更有效的傳遞資訊,對與那些沒有參與到統計結果的表格設計和表達的非統計學人員來說,圖形所傳遞的資訊更容易被接受。統計結果視覺化可以提升臨床試驗過程中的合作品質,縮短時間和決策,尤其是當研究問題比較複雜的時候,有作者專門就圖形設計而撰文。
不良事件視覺化評價應當具備以下關鍵要素:1.將必要的統計量整合到圖形中,2.在圖形中加入適當的指示線,3.通過圖形能直觀的比較試驗組和對照組的差異,4.便於進行不良事件之間的相互比較,5.圖形應能突出顯示需要重點關注的不良事件。
- 資料來源及繪圖軟體:
本研究資料來源於一項治療蛛網膜下腔出血病人的隨機雙盲安慰劑對照的Ⅲ期臨床試驗,該評價藥物的作用機制主要為通過阻滯鈣通道,抑制平滑肌收縮,擴張血管。該研究共入組病人906例,其中藥物組449例,安慰劑組457例,兩組之間平衡了可能影響預後的因素,兩組病人持續服藥14天,每天0.15 mg/Kg/hr,隨訪120天觀察結果。
JMP Clinical是專門面向臨床試驗資料分析而開發的統計軟體,其採用標準的CDISC資料格式,將高級統計方法和豐富的互動式圖形結合起來,在使用者友好的環境中提供了強大的統計分析能力。SAS本身也具備繪圖功能。文中所繪製圖形均採用SAS以及JMP Clinical。
3.不良事件的視覺化表達方法
3.1描述不良事件發生率和組間相對危險度(Relative Risk, RR)
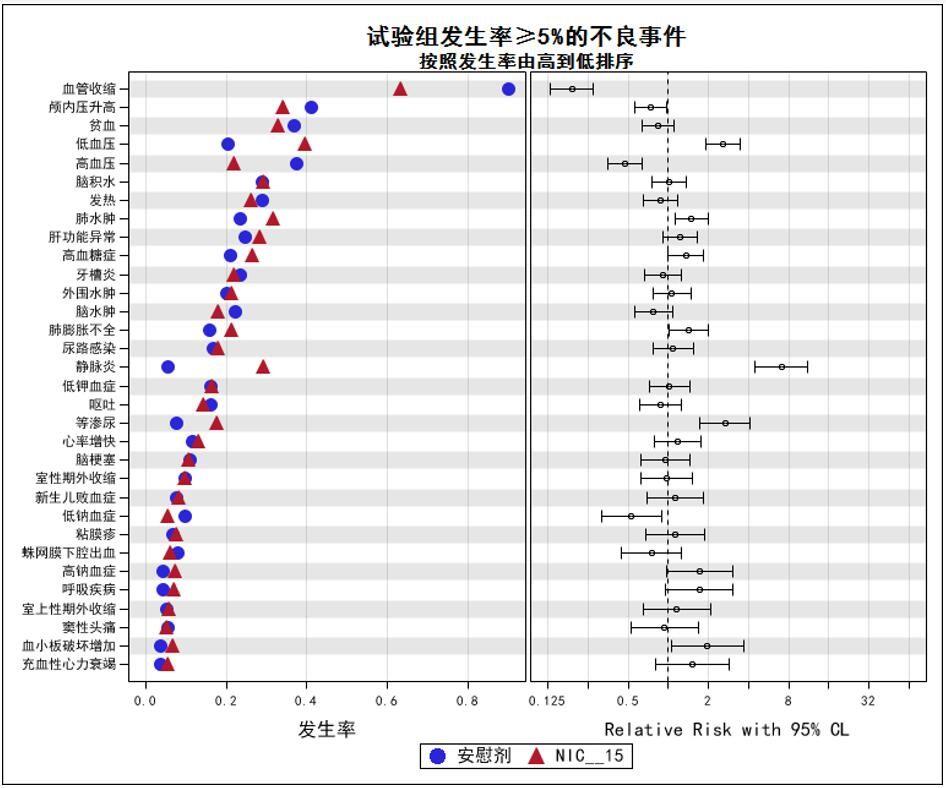
不良事件發生率是描述不良事件發生情況最常用的度量,RR則反映了不良事件發生率在試驗組合對照組之間的差異。運用森林圖的原理,把不良事件發生率、RR及其95%置信區間整合到一幅圖中,既可以觀察到各組的不良事件發生率,又可以根據RR及其95%置信區間推斷組間差異有無統計學意義,還可以縱向進行不同種類不良事件之間的比較。根據研究目的,在森林圖中按照一定規律對不良事件進行排序,可以直觀、突出的顯示最需要關注的不良事件。例如在臨床研究中,目的是描述發生率較高的不良事件,就應該按照發生率由高到低排序。
該研究過程中共觀察到201種不良事件,文中選取試驗組發生率≥5%的不良事件,並按照發生率由高到低排序繪製圖1。 圖中左側圖版的散點表示不良事件的發生頻數,紅色三角代表試驗組,藍色圓點代表對照組;右側版圖表示該不良事件試驗組相對於對照組的RR及其95%可信區間。X軸上的刻度進行log2轉換,虛線的位置為刻度0,相當於RR=20=1;刻度為1的位置相當於RR=21=2,依此類推。從圖中可以觀察到:試驗組發生率高於對照組且差異具有統計學意義的不良事件分別是“靜脈炎”、“等滲尿”、“低血壓”和“肺水腫”;對照組發生率高於試驗組且差異具有統計學意義的不良事件分別是 “高血壓”、“血管收縮”和“低鈉血症”。
按照森林圖的原理繪圖,需要把每種不良事件作為一列,而一項臨床試驗中可能會有上百種不良事件,所以在實際應用中應該結合視覺化目的,選擇重點關注的部分不良事件來作圖,選擇的標準要經過認真考慮。本文中選取發生率≥5%的常見不良事件,這樣選取存在另外一個問題:可能會有某種不良事件,其發生率<5%,但組間差異卻有統計學意義,如果按照發生率來篩選,可能會把這樣的不良事件遺漏。
圖 1不良事件發生率及相對風險圖
3.2描述機體系統分類、不良事件發生數目以及組間差異
不良事件系統分類是不良事件分析的必要內容,目前常以表格的方式描述各系統的不良事件發生率,採用樹圖則可以將不良事件系統分類、各不良事件發生率以及組間差異的統計學意義整合到一幅圖中。樹圖是基於層次的視覺化技術的代表技術,其基本思想是將n維資料空間劃分為若干子空間,對這些子空間仍以層次結構的方式組織並以圖形表示出來。
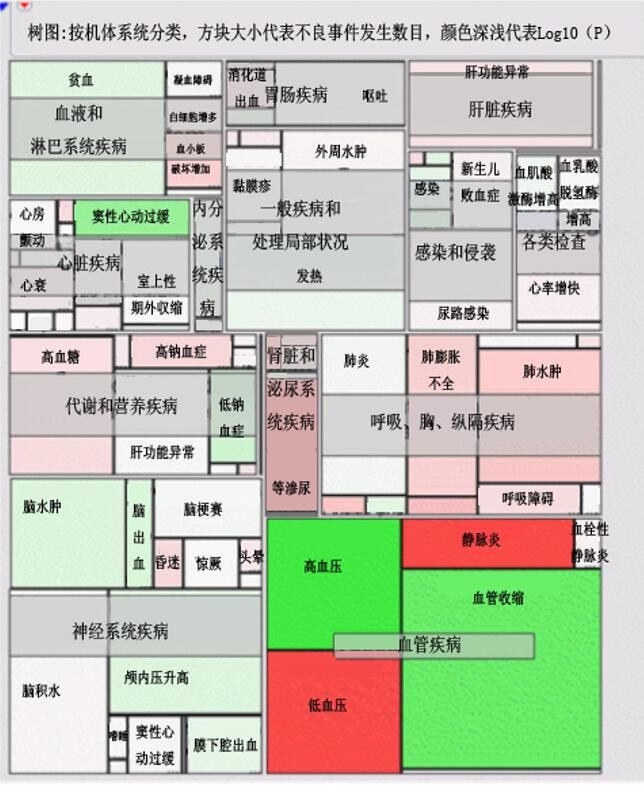
根據以上原理繪製圖2,圖中每一個方塊代表一種不良事件。同一系統的不良事件排列在一起,並以半透明的方式標記其系統歸類名稱。方塊大小與此類不良事件發生數成正比,方塊越大表示該種不良事件總發生數目越多,反之方塊越小則表示該種不良事件發生數越少。方塊的顏色為紅色表示該不良事件試驗組發生數目多於對照組,綠色表示該不良事件對照組發生數目多於試驗組。方塊顏色深淺與該不良事件發生數目由組間差異P值決定,P值越小,顏色越深,代表組間差異顯著性越高。
圖2 樹圖
這種圖形表達方式可以給讀者以強烈的視覺衝擊,讀者可以直接看到顏色最深的方塊的表示該不良事件組間差異非常顯著,這種差異很可能是由於處理措施造成的;此外讀者還可以直觀的觀察不良事件的發生總數、不良事件的組間差異等資訊,這些資訊的獲取都是簡單、直接的,是用數位表格無法比擬的。圖中可以觀察到, “神經系統疾病”與“血管疾病”的發生率大致相同,但是“血管疾病”組間差異顯著性遠高於“神經系統疾病”。“血管疾病”主要是四種不良事件,其中“靜脈炎”和“低血壓”在試驗組中的發生率高與對照組;而“血管收縮”和“高血壓”在對照組中的發生率高於試驗組。
圖2由JMP繪製,在該軟體中可以直接點擊感興趣的不良事件方塊,對該不良事件進行統計描述或者統計推斷,從而得到需要的具體數值。臨床研究的目的往往不盡相同,實際應用中可以在圖2的基礎上進行適當變換,比如可以分組輸出兩個樹圖等。
3.3篩選組間差異有統計學意義的不良事件
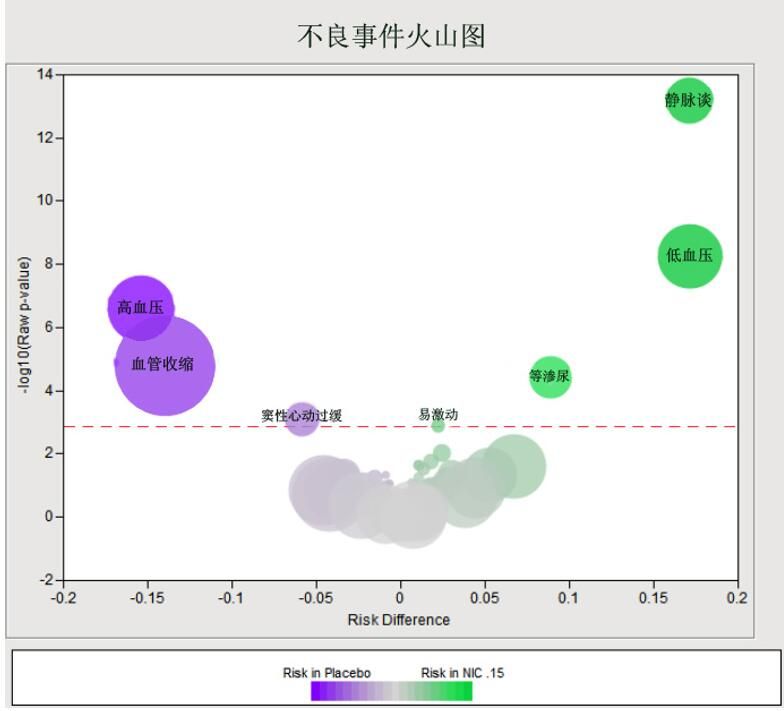
篩選組間差異有統計學意義的不良事件,明確其與用藥的關係是不良事件分析的主要目的之一,應用火山圖可以幫助研究者迅速找到具有組間差異有統計學意義的不良事件,然後對這些不良事件進行細緻的分析。在統計學中,火山圖是通過散點圖的形式快速識別大型資料集中同類型資料的組間差異。跟據以上原理繪製圖3,不僅突出顯示組間差異有顯著性的不良事件,還同時顯示這些不良事件的總發生率和組間發生率差(Risk Difference, RD)。
圖中X軸表示所發生不良事件在試驗組與對照組間的率差(試驗組-對照組),Y軸表示組間差異的統計學意義。RD大於0的點表示該不良事件試驗組發生較多,小於0的點表示該不良事件對照組發生較多,偏離0點越遠表明組間差異越大。Y軸表示組間差異的顯著性,點在Y軸上的數值越大代表該不良事件組間差異的P值越小,統計學意義上的顯著差別通過SAS混合模型計算、並採用了統計中的錯誤發現率(False Discover Rate: FDR)多重檢驗校正所得。經過校正以後,在紅色虛線以上的不良事件有組間統計學差異。點的顏色所代表的意義如圖例所示,點的大小則代表不良事件發生率。
圖 3反映不良事件組間差異以及差異大小的火山圖
3.4不良反應合併發生情況
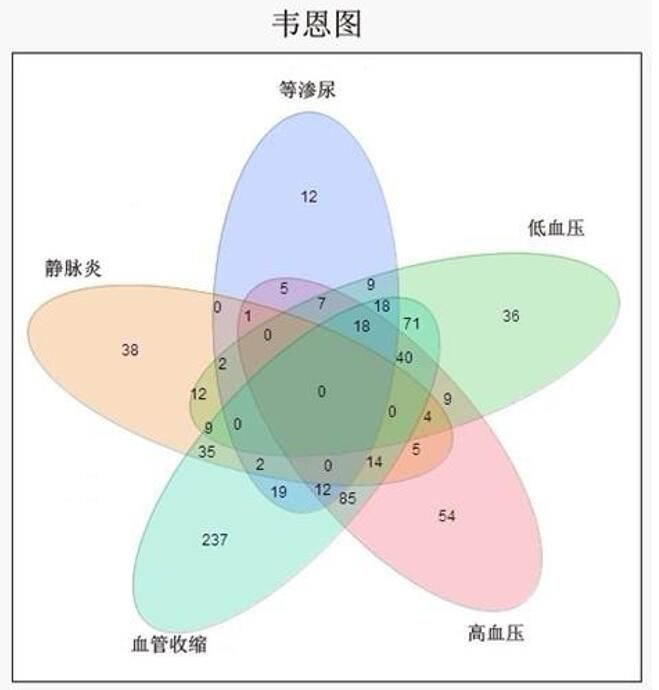
通過火山圖觀察到需要重點關注的不良事件主要有5種,此時研究者往往需要細緻的分析這5種不良事件,其中包含通過觀察不良事件的併發情況推斷其發生原因。針對此目的可以使用韋恩圖或稱文氏圖(Venn diagram),統計學中,韋恩圖是用一條封閉曲線直觀的表示集合及其關係的圖形。
圖 4韋恩圖
3.5 長期隨訪臨床研究中需要對AE資料進行存活分析
不良事件的統計分析中,為了觀察隨著時間變化受試者發生某不良事件的風險,可以把不良事件資料作為time – to – event資料進行存活分析。 採用存活分析模型來評價事件發生的風險是非常合適的,因為不良事件資料本身既包含發生情況(有或無),也包含事件發生時間,在長期治療中會有相當比例的截尾值,所以應當採用存活分析計算不良事件累積率,以免低估風險。ICH推薦使用存活分析方法分析不良事件資料,已有國外文獻論證存活分析模型在不良事件分析中的意義,並對存活曲線的設計進行了探討。臨床研究中不良事件種類較多,該方法只能對某一重點關注的不良事件作存活分析。
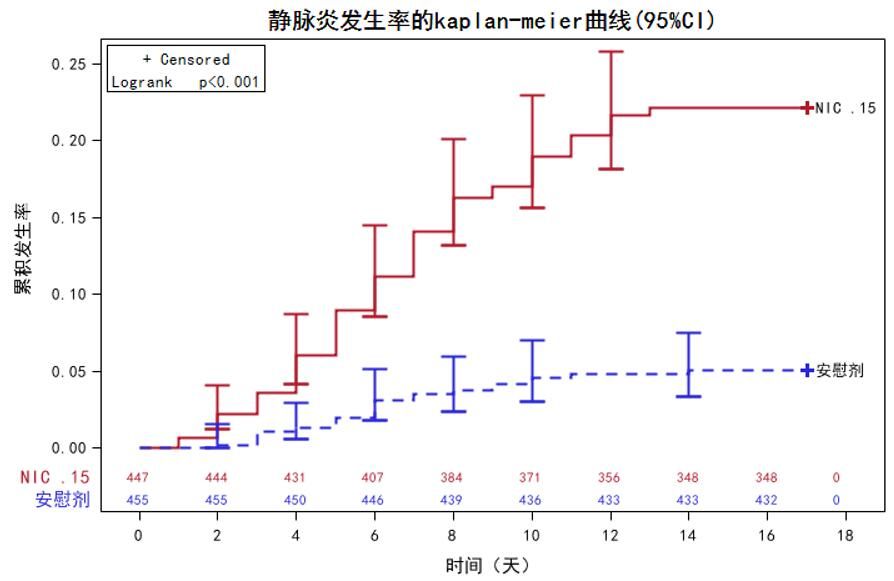
不良事件分析中關注的是不良事件發生時間與用藥時間的關係,圖5是兩組靜脈炎發生時間的Kaplan-Meier曲線,圖中下方的數字表示每次訪視的期初人數,曲線上的“+”表示在此時刻有刪失病例,曲線上下繪製95%可信區間。如果兩條曲線非常接近,再繪製可信區間,就會使兩條曲線難以區分,為了保持圖形簡潔、易分辨,建議可以採取以下方法:1.用標準誤代替95%可信區間,或只繪製出曲線上方的標準誤,2將試驗組曲線向左移動,安慰劑組曲線向右移動,使兩條曲線的可信區間交錯排列,3不再繪製可信區間,在圖中標記HR及其可信區間或Log-rank檢驗的P值即可。
圖 5 靜脈炎發生時間的Kaplan-meier曲線
圖中可以得知,靜脈炎集中在研究開始後17天內發生,主要集中在前14天內,這與研究的用藥時間是相符合的,而且試驗組靜脈炎的發生速度遠超過安慰劑組,提示該藥物在用藥期間可能誘發靜脈炎。
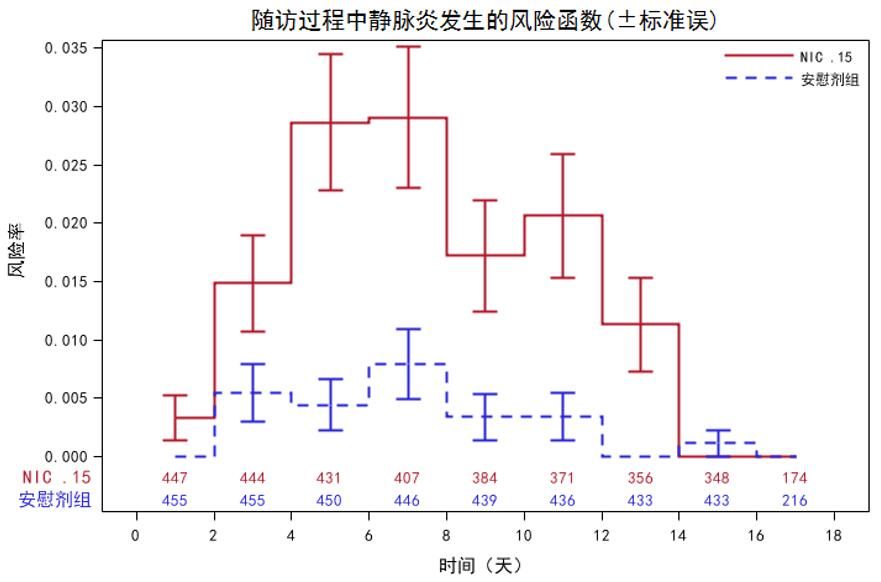
除存活函數以外,存活分析中還可以通過壽命表法計算風險函數,圖6繪製了隨訪過程中靜脈炎的風險函數圖。同樣的,在圖形下方標注期初人數,並在曲線上繪製了標準誤。該圖採用壽命表法計算,並設置兩天為一個區間,每一個區間的風險率為該區間中點時刻的風險率。該圖直接反映了用藥後不同時刻受試者發生靜脈炎的風險。需要注意的是:由於SAS中壽命表法假設所有刪失病例都是發生在時間區間的中點,相當於刪失病例只經歷了時間區間的一半,所以在計算期初人數的時候,刪失病例要乘以0.5。這樣就會導致期初人數可能不是整數。
圖 6不良事件風險函數圖
在長期隨訪的臨床試驗不良事件評價中,推薦使用以上兩幅圖。
4.討論
臨床試驗中不良事件分析的方向很多,文中儘量從多個角度進行分析展示,但是仍然不能面面俱到。以上6幅圖不僅僅可以適用于文中展示的分析目的, 例如臨床試驗中會遇到這樣的問題“如果病人治療了X個月未出現不良事件,我們能放鬆警惕嗎?我們必須保持多長時間的警惕性?”,根據這個需要,可以應用圖5對不良事件的首次發生時間做風險函數圖,然後圖中可以觀察到經過X個月以後風險率降為0,即在X個月之內要保持警惕。總之,在不良事件視覺化分析的過程中,一定要將視覺化目的與圖形的特點結合起來,選擇最合適的圖形。
臨床試驗兩組中某一組不良事件發生頻數為0的情況較常見,對於這類資料,常用的方法是每個格子加上0.5,然後計算RR,或者使用率差(risk difference,RD)。本文中採用率差進行統計。
不良事件的分析中也應該考慮不良事件發生的一些潛在影響因素,比如病程、年齡、性別、病情輕重、服藥量等,可以採用logistic回歸分析,把相關因素作為協變數,計算OR值,用OR值繪製圖1。不良事件為0頻數比重較大,不良事件發生頻數的方差大於均數以及不良事件發生的聚集性即發生了一次不良事件再發生不良事件概率改變的這三個特點,使得不良事件比較適合用負二項回歸進行模型擬合。所以Logistic回歸不適用的時候,可以考慮負二項回歸模型。
如果對臨床試驗中不良事件的組間差異進行統計學檢驗,則要考慮到多重比較的問題,降低假陽性錯誤。傳統的多重比較是基於控制總Ⅰ型錯誤率,但在組數過多時其結果過於保守,基於控制陽性結果錯誤率的方法既能獲得較高的檢驗效能, 又能較好地控制總Ⅰ型錯誤率。
5.總結
新藥上市以前,必須通過科學的、規範的、按照GCP要求的臨床試驗證實其有效性和安全性,不良事件的分析是安全性評價的重要方面,因此顯的尤為重要。然而當前對不良事件的分析並不完善,當然這也與安全性分析的特點有關,因為安全性評價不同於有效性評價,對於有效性評價,要事先在研究方案中明確有臨床試驗終點,通過不同組間結果比較的的假設檢驗,來關注目標人群的平均反應;而安全性終點通常不會事先確定,從性質上看,安全性分析更傾向於是探索性的。相對於臨床療效分析看重平均值;安全性評價更看重個體的反應。這就決定了不良事件分析主要是以統計描述的形式進行的。
然而目前以表格為主的統計描述,表格數量繁多難以有效傳達資訊。採用視覺化的方法對不良事件進行分析,不僅簡潔、目標指示明確,而且把可以相關的主要統計量整合在圖形中,提高溝通效率,節省研發時間。因此臨床試驗的不良事件分析中,建議採用視覺化分析方法通過繪製不同統計圖形發現潛在的安全性信號。
- © 2024 JMP Statistical Discovery LLC. All Rights Reserved.
- Terms of Use
- Privacy Statement
- About JMP
- JMP Software
- JMP User Community
- Contact
You must be a registered user to add a comment. If you've already registered, sign in. Otherwise, register and sign in.